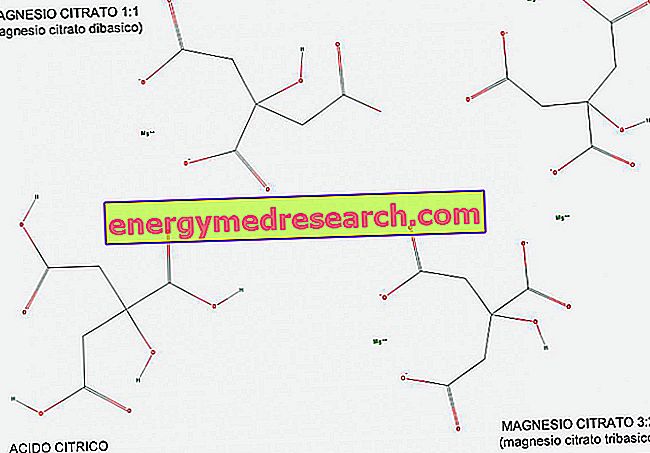
Tribasiline (või triprootiline) hape on hape, millel on happe-aluse reaktsioonis annetamiseks kolm vesinikiooni. Joonise abil näeme, kuidas sidrunhape on tribashappe näide, kuna sellel on kolm COOH karboksüülrühma, mis võivad vesiniku H. kergesti üle kanda.
Magneesiumtsitraat on nii 1: 1 proportsioonis (1 magneesiummolekul tsitraatmolekuli kohta) kui ka 3: 2 proportsioonis (3 magneesiummolekuli 2 tsitraatmolekuli kohta).
1: 1 nimetatakse magneesiumtsitraati kahealuseliseks, sest see on sidrunhappe kahealuseline sool; tegelikult on sellel molekulil kaks ühevalentset põhirühma (COO-), mis on tuletatud kahest karboksüülrühmast, mis on reaktsiooni ajal oma vesiniku loobunud.
3: 2 nimetatakse seevastu magneesiumi tribasiliseks, sest sellel on 3 ühevalentset põhirühma (COO-) molekuli kohta, mis on tuletatud 3 karboksüülrühmast, mis andsid reaktsiooni ajal oma vesiniku.
Tribasiline magneesiumtsitraat on magneesiumis (+ 42, 6 massiprotsenti) selgelt mitmekesisem kui kahealuseline magneesiumtsitraat; pealegi on see rohkem leelistav, kuna see võib vastu võtta kolm vesiniku iooni H + kahe kahemõõtmeliste poolt aktsepteeritud. Siiski on see vees vähem lahustuv.